Prise en charge de la maladie valvulaire dégénérative mitrale du chien
Dr Anne-Charlotte BARROT (CHV Saint-Martin)
La maladie valvulaire dégénérative mitrale (MVD) est la maladie cardiovasculaire la plus fréquente chez le chien. Lorsque la régurgitation devient importante, la compensation cardiaque se manifeste par une surcharge volumique gauche (augmentation de l’atrium et du ventricule gauche). Elle précède l’insuffisance cardiaque congestive (ICC) gauche à l’origine de l’œdème pulmonaire cardiogénique. A partir du stade C (ie chien ayant eu et/ ou présentant des signes cliniques de décompensation cardiaque) et en dépit de l’efficacité des traitements recommandés, la survie médiane de ces chiens est inférieure à 1 an (The QUEST study, JVIM 2008). Il est donc primordial de retarder au maximum ce stade.
1- RAPPEL de la classification et des recommandations (d’après le Consensus ACVIM 2009)
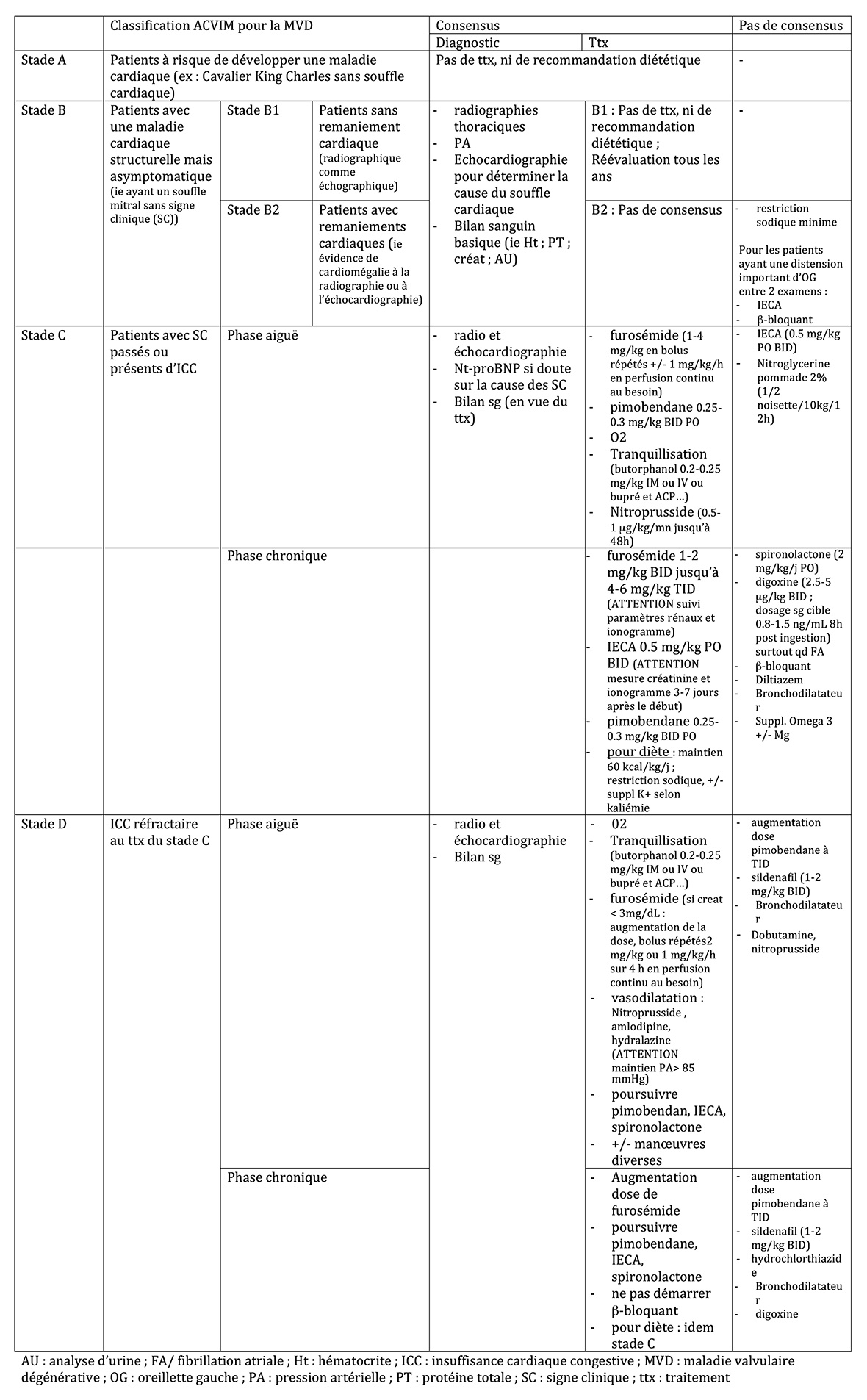
Le consensus n’avait établi aucune recommandation concernant la mise en place d’un traitement avant le stade C.
Le but de l’étude EPIC (Boswood A., Häggström J., Gordon SG. et al. Effect of pimobendan in dogs with preclinical myxomatous mitral valve disease and cardiomegaly : the EPIC study- A randomized clinical trail. J Vet Intern Med. JVIM 2016) était d’investiguer le ou les potentiel(s) intérêt(s) de la mise en place du pimobendane en stade B2 (ie avant le premier épisode d’œdème pulmonaire).
2- Résumé de l’étude EPIC
2.1. Matériel et méthodes
L’étude EPIC est une étude prospective, multicentrique, randomisée et double aveugle. Les chiens ont donc été répartis à l’aveugle entre le groupe « placebo » (témoin) et le groupe « pimobendane ». Le recrutement a été fait entre octobre 2010 et juin 2013 dans 36 cliniques vétérinaires à travers le monde. Les comprimés de pimobendane ou de placebo avaient le même aspect. La dose de pimobendane était la dose conventionnelle ie 0,4 à 0,6 mg/kg/j divisée en 2 prises à 12h d’intervalle et n’était pas ajustée pendant l’étude.
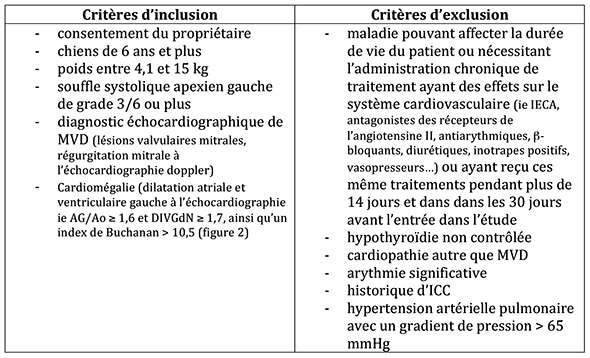
Les critères d’inclusion et d’exclusion de l’étude sont résumés dans le tableau 1.
DIVGdN : diamètre du ventricule gauche en diastole normalisé avec le poids ; MVD : maladie valvulaire dégénérative
Chaque chien dans un groupe et ayant reçu au moins une dose était inclus dans la population « intention de traiter » (ITT). Tout chien dans la population ITT qui avait été confirmé comme répondant à tous les critères d’inclusion était inclus dans la population per protocole (PP) jusqu’à ce que l’un des éléments suivants se soit produit : chien ayant atteint le critère d’évaluation principal, chien ayant été censuré de l’analyse en raison d’un non-respect du protocole ou fin de l’étude étant atteinte.
Le critère d’évaluation principal était l’apparition d’un des évènements suivants :
- ICC gauche
- Euthanasie en raison d’un problème cardiaque confirmé sur la base des signes cliniques et des radiographies thoraciques
- Mort considérée comme secondaire à la maladie cardiaque ie si aucune autre cause non cardiaque n’était apparente
Pour les critères d’évaluation secondaires, un chien était considéré comme ayant vécu un événement si l’une des situations suivantes se produisait :
- Chien ayant atteint le critère d’évaluation principal
- Mort ou euthanasie sans lien avec la maladie cardiaque
- Chien nécessitant un traitement chronique avec un médicament ayant des effets sur le système cardiovasculaire, un antitussif, un bronchodilatateur ou un glucocorticoïde
- ICC gauche ne pouvant être confirmée
- Chien étant retiré de l’étude sur demande du vétérinaire ou du propriétaire
- Protocole de suivi ou de traitement non respecté
Pour chaque chien inclus, les éléments suivants étaient collectés au début de l’étude : commémoratifs et anamnèse, examen clinique, mesure de PA, hémogramme, ALT, PT, créatinine, K+, Na+, radiographies thoraciques et échocardiographie complète. Un suivi a été fait après 35 jours, puis après 4 mois et enfin tous les 4 mois.
Une analyse statistique intermédiaire, prévue après 80 % du temps estimé de l’étude, a permis d’arrêter de manière prématurée l’étude (ie avant d’avoir atteint les 150 cas de chaque groupe), en raison de preuves évidentes d’efficacité établies sur le critère d’évaluation principal (p< 0,01477).
2.2. Résultats
- 360 chiens inclus ; âge médian : 9 ans
- pas de différence significative dans la composition des 2 groupes
- 192 chiens ont été censurés de l’analyse du critère d’évaluation principal dont 54 dans le groupes « pimobendane » et 29 dans le groupe « placebo » car ils étaient toujours en vie à la fin de l’étude sans atteindre le critère d’évaluation principal (durée médiane de l’étude pour ces chiens : 1056 jours).
- 162 chiens (45,8%) ont atteint le critère d’évaluation principal
- pas de différence significative entre les 2 groupes au niveau du nombre
- différence significative entre les 2 groupes pour le temps médian pour atteindre le critère d’évaluation principal : 1228 jours pour le groupe « pimobendane » et 766 jours pour le groupe « placebo », ie enviorn 15 mois, idem si on ne considérait que ICC gauche (1337 versus 846 jours)
- médiane de survie toutes causes de mortalité différentes était significativement différente entre les 2 groupes : 1059 jours pour le groupe « pimobendane » et 902 jours pour le groupe « placebo »
- absence d’effet indésirable significatif du pimobendane dans cette étude
3- Conclusion
L’étude EPIC est la première étude prospective à montrer l’efficacité d’un médicament en phase préclinique de MVD mitrale en prolongeant significativement la durée avant l’apparition ICC gauche. Le pimobendane prolonge donc la durée de vie des chiens atteints de MVD mitrale.
Cette étude démontre qu’un traitement à base de pimobendane doit être proposé dès le stade B2 de la MVD mitrale.